Chuyên đề 1. Enzym, vitamin và các nguyên tố vi lượng trong cơ thể
1. Enzym
Enzym là các protein có tác dụng xúc tác sinh học, xúc tác hơn 5.000 loại phản ứng hóa sinh, một số được cấu thành từ phân tử RNA được gọi là ribozym (từ những năm 1980, người ta nhận biết khả năng xúc tác của loại này, tuy nhiên rất ít thông tin về hoạt động của chúng). Trong phạm vi bài viết này chỉ tập trung vào các enzym bản chất là protein. Có khoảng 1300 loại enzym khác nhau được tìm thấy trong tế bào người.
Enzym có đầy đủ tính chất của chất xúc tác , đó là : (i) làm tăng tốc độ phản ứng bằng cách làm giảm năng lượng hoạt hóa, một số enzym có khả năng tăng tốc độ phản ứng nhanh hơn tới hàng triệu lần, như orotidine 5′-phosphate decarboxylase; nó có khả năng kích hoạt một phản ứng kéo dài hàng triệu năm chỉ trong vòng vài mili giây, (ii) không làm thay đổi sự cân bằng hóa học, không thay đổi chiều của phản ứng , không tạo ra phản ứng. (iii) không bị tiêu thụ trong các phản ứng hóa học . Enzym có tính đặc hiệu cao, bị ảnh hưởng bởi các ức chế và các chất hoạt hóa enzym. Nhiều thuốc và thuốc độc trên thực tế là chất ức chế enzym.,
Sự tổng hợp enzym chịu sự kiểm soát và phân phối di truyền trong tế bào. Các tế bào ở các cơ quan, mô khác nhau có các kiểu biểu hiện gen khác nhau và vì vậy ở đó có các bộ enzym khác nhau đê sẵn sàng cho các phản ứng trao đổi chất. Một số enzym không được tổng hợp ở một số tế bào, và một số enzym khác chỉ được hình thành khi có nhu cầu. bởi vậy các enzym không phải lúc nào cũng tồn tại đồng nhất trong một tế bào. Tốc độ tổng hợp và hoạt động của các enzym còn chịu ảnh hưởng bởi các hormone, các hoạt động thần kinh và các chất hóa học khác ảnh hưởng đến môi trường bên trong của tế bào. Trong quá trình tổng hợp, sau giai đoạn dịch mã thành protein, tiếp theo là sự biến đổi sau dịch mã. Ví dụ Chymotrypsin, một protease tiêu hóa, được sản xuất ở dạng không hoạt động dưới dạng tiền chất chymotrypsinogen (gọi chung là zymogen) trong tuyến tụy và dạng này được vận chuyển đến dạ dày, ở đó nó được kích hoạt bởi trypsin để thành chymotrypsin .
Thông qua hoạt động xúc tác, enzyme có tác dụng truyền tín hiệu và điều hòa tế bào như các kinase và phosphatase. Enzym cũng tạo ra chuyển động như myosin , một protein của cơ, hoạt động như một enzym ATPase, thủy phân ATP để tạo ra sự co cơ . Enzym tham gia các vào quá trình vận chuyển tích cực như các ATPase trong màng tế bào có vai trò là các bơm ion. Trong hệ thống tiêu hóa các enzym phá vỡ các phân tử lớn thành các phân tử nhỏ hơn để hấp thu .
Trong con đường trao đổi chất, các enzym hoạt động nối tiếp nhau trong chuỗi các phản ứng chuyển hóa và được điều chỉnh ở một số bước quan trọng để thúc đẩy chuỗi phản ứng trao đổi chất liên kết một cách tổng thể.
Hiệp hội quốc tế về Hóa Sinh (International Union of Biochemistry – IUB,)đã thiết lập bảng phân loại và danh pháp enzym ( bảng 1.1) . Theo đó các enzym được chia thành 6 nhóm, ghi theo các chữ số 1 – 6, mỗi nhóm lại chia thành dưới nhóm được biểu thi bằng chữ số thứ hai , và tiếp tục chia thành các nhóm nhỏ hơn, biểu thị bằng chữ số tiếp theo…. Mỗi enzym có tên biểu thị ký hiệu bằng các chữ số, Thí dụ enzym Lactat dehydrogenase sẽ có ký hiệu LDH (EC 1.1.1.27),là enzym thuộc nhóm 1. Enzym oxy hóa khử, dưới nhóm 1.1. thuộc phân nhóm dehydrogenase…
Bảng 1. Phân loại Quốc tế enzym
| Loại | Tên enzym | Chức năng | Phản ứng tổng quát |
| 1 | Enzym oxy hoá khử (oxidoreductase) | Vận chuyển điện tử, xúc tác cho phản ứng oxy hoá và phản ứng khử | AH2 + B -> A + BH2 |
| 2 | Enzym vận chuyển nhóm (transferase) | Vận chuyển một nhóm hoá học (không phải là H2) | AX+B -> A+BX |
| 3 | Enzym thuỷ phân (hydrolase) | Cắt liên kết của chất hoá học bằng cách thuỷ phân ( có sự tham gia của H2O) | AB + H2O => AH + BOH |
| 4 | Enzym phân cắt (lyase) | Tách nhóm hoá học ra khỏi cơ chất không có sự tham gia của H2O | AB => A+B |
| 5 | Enzym đồng phân
(isomerase) |
Xúc tác phản ứng biến đổi giữa các dạng đồng phân của chất hoá học | ABC => ACB |
| 6 | Enzym tổng hợp
(ligase hoặc synthethase) |
Xúc tác phản ứng gắn 2 phân tử sử dụng ATP hoặc các NTP khác để cung cấp nắng lượng | A + B + ATP => AB
+ ADP+Pi |
1.1. Sự phân bố enzym trong cơ thể
1.1.1. Enzym nội bào
Enzym tồn tại hầu hết trong mọi mô mọi tế bào. Các enzym tổng hợp và hoạt động trong tế bào được gọi là enzym nội bào. Các enzym nội bào khu trú trong các thành phần của tế bào. Các enzym này không rời khỏi tế bào, chúng được giữ lại bên trong các khu vực của tế bào, chúng được tìm thấy trong tế bào chất, trong lysosom , ti thể, nhân, vv.. để sử dụng nội bộ, cho các phản ứng hóa sinh xảy ra trong tế bào. như các enzym xúc tác quá trình đường phân , quá trình sinh tổng hợp protein , tổng hợp acid nucleic… Enzym trong các mô khác nhau về số lượng phụ thuộc vào giai đoạn sinh trưởng phát triển của tế bào, khác nhau cả về chất lượng , đó là tính đa dạng của enzym . Các enzym này có nhiều dạng khác nhau cùng xúc tác một phản ứng hoá học nhưng có bản chất xúc tác khác nhau vì các enzym đó được mã hoá bởi các gen có locus khác nhau trên NST tạo nên sự đặc hiệu cơ quan. ( các isozym khác nhau trong các mô khác nhau). Điển hình về tính đa dạng được nhắc tới là Các isozym LDH. LDH được tạo thành thừ hai chuỗi polypeptid, Chuỗi H và chuỗi M.Chuỗi H được thấy chủ yếu ở cơ tim, chuỗi M chủ yếu trong cơ xương và gan.. Các chuỗi nà tạo thành 5 dạng phân tử tetrame LDH1 (HHHH), LDH2 ( HHHM, LDH3 (HHMM) , LDH4 (HMMM) và LDH5 (MMMM). Mô tim nhiều LHH1 LDH2, Mô cơ xương nhiều LDH 3 và LDH4, gan nhiều LDH5.
Mỗi cấu trúc dưới tế bào có chức năng riêng nên có sự sắp xếp hợp lý trong từng phần dưới tế bào để phối hợp các tác dụng của các enzym trong một dây truyền phản ứng.
- Loại khu trú trong bào tương gồm nhiều loại enzym chuyển hóa carbohydrat, lipid, acid amin…như: lactatdehyrogenase (LDH), alanin transaminase (ALT)… trong ty thể như: glutamat dehydrogenase (GLDH),… aspartat transaminase (AST) cả trong bào tương và ty thể.
- Loại khu trú trong nhân tế bào có lượng enzym rất ít, là các enzym loại nicotinic tham gia các chuyển hóa liên quan đến trao đổi nucleic.
- Loại khu trú trong ty thể, trước hết phải nói tới hệ thống enzym của chuỗi hô hấp tế bào nằm ở màng trong của ty thể, các enzym của chu trình Krebs, các enzym xúc tác quá trình kéo dài chuỗi acid béo.
- Loại khu trú trong lysosom gồm các enzym hydrolase thủy phân các phân tử lớn thành các phân tử nhỏ hơn, thí dụ phosphatase acid…
1.1.2. Enzym ngoại bào
Enzym ngoại bào là các enzym sau khi đươc tổng hợp trong tế bào, chúng được tiết ra bên ngoài tế bào để thực hiện các phản ứng hóa học bên ngoài tế bào. Các enzym này xúc tác cho các phản ứng sinh hóa xảy ra bên ngoài tế bào. Enzym tiêu hóa một loại enzym ngoại bào. Chúng được tiết ra bởi các tế bào chuyên biệt của ruột, của tụy. Chúng hoạt động trên thức ăn trong hệ tiêu hóa.
1.1.3. Các enzym trong huyết tương
Có thể hiểu các enzym trong huyết tương bao gồm:
+ Enzym đặc hiệu huyết tương (plasma-specific enzymes): Các enzym này thể hiện chức năng đặc hiệu của chúng trong huyết tương. VD: các enzym đông máu (prothrombin, yếu tố V, yếu tố VII…)
Cũng có một số enzym được coi như hoạt động trong huyết thanh như Lipoprotein lipase (LPL) enzyme hòa tan trong nước LPL được tiết ra từ các tế bào nhu mô ở tim, cơ và mỡ dưới dạng homodimer được glycosyl hóa, sau đó di chuyển qua chất nền ngoại bào và tế bào nội mô đến mạch máu, gắn vào bề mặt sáng của tế bào nội mô trong mao mạch bởi protein glycosylphosphatidylinositol HDL-binding protein 1 (GPIHBP1) và bởi peptidoglycans heparan sulfat, LPL có tác dụng thủy phân triglycerid trong chylomicrons và lipoprotein mật độ rất thấp (VLDL) giải phóng hai acid béo tự do và một phân tử monoacylglycerol
+ Các enzym được bài tiết (secreted enzymes):Các enzym không có chức năng đặc hiệu trong huyết thanh VD: leucin aminopeptidase, phosphatase kiềm của gan, lipase, amylase của tụy, phosphatase acid của tuyến tiền liệt.
Nồng độ của các enzym này bình thường trong huyết thanh rất thấp, nó là kết quả của sự thay cũ đổi mới của tế bào. Nồng độ sẽ tăng lên khi tổn thương tổn thương tế bào. Việc hiện diện các enzym này trong huyết thanh rất được quan tâm trong chẩn đoán và theo dõi bệnh. Xác định hoạt độ các enzym trong huyết thanh là một trong các xét nghiệm giúp các nhà lâm càng chẩn đoán theo dõi bệnh.
Bảng 2 Chu kỳ bán hủy của các enzym trong huyết thanh
| Enzym | Thời gian bán huỷ |
| ALP | 3-7 ngày |
| α-amylase | 9-18giờ |
| ALT (GPT) | 47 giờ |
| AST (GOT) | 17± 5 giờ |
| CHE | 10 ngày |
| CK | 12giờ |
| CK-MM | 20giờ |
| CK-MB | 11±1 giờ |
| CK-BB | 2-4 giờ |
| GLDH | 14.2 ± 0.77giờ |
| GGT | 17 – 26 ngày |
| LDH1 (α-HBDH) | 4-5 ngày |
| LDH5 | 10 giờ |
| Lipase | 7-14 giờ |
+ Thời gian bán huỷ của các enzym trong huyết tương khác nhau nên việc sử dụng kết quả đo hoạt độ các enzym trong chẩn đoán có sự khác nhau
+ Ngoài cơ thể: giảm 0-5% sau 24h, 10% sau 48h ở 4oC, còn 85-100% sau 48h ở 25oC.
1.2. Định lượng hoạt độ enzym
Nồng độ các enzym không được định lượng trực tiêp mà gián tiếp qua độ họat động xúc tác của chúng.
Đơn vị hoạt độ xúc tác của enzym được thống nhất và biểu thị bằng
- Đơn vị Quốc tế ( U : International Unit). Một đơn vị Quốc tế được xác định là lượng enzym nào đó xúc tác chuyển đổi 1 micromol cơ chát thành sản phẩm trong thời gian 1 giây trong những điều kiện xét nghiệm nhất định. Thường được biểu thị bằng đơn vị U trong 1 lít : U/L
1U = 1 μmol/phút
- Đơn vị Katal ( ký hiệu Kat) 1 Katal được xác định là lượng enzym nào đó xúc tác chuyển đổi 1 mol cơ chát thành sản phẩm trong thời gian 1 phút trong những điều kiện xét nghiệm nhất định.
1 Kat = 1mol/ giây.
Hai đơn vị này chuyển đổi sang nhau: 1 μKatal/ L = 60 U/L
1.3. Ý nghĩa lâm sàng của các xét nghiệm enzym
Dựa vào, nguồn gốc, nơi khu trú mức độ hoạt động của enzym để phát hiện tổn thương của mô và cơ quan tổ chức
Bảng 1.3. Một số enzym chính dùng trong lâm sàng
| Enzym | Ý nghĩa lâm sàng |
| Phosphatase acid ( ACP) | Ung thư tuyến tiền liệt |
| Alaninamino transferase (ALT) | Bệnh lý gan |
| Aldolase (ALD) | Bệnh lý cơ xương |
| Alkalin phosphatase(ALP) | Bệnh lý gan
Bedenhj lý xương |
| Amylase ( AMS) | Viêm tụy cấp |
| Aspartat amino transferase (ÁST) | Nhồi máu cơ tim
Bệnh lý gan Bệnh lý xương |
| Creatinkinase ( CK) | Bệnh lý cơ xương Nhồi máu cơ tim |
| Glutamat dehydrogenase ( GlDH) | Bệnh lý gan |
| Gama glutamyl trán ferase ( GGT) | Bệnh lý gan |
| Lactatdehydrogenase ( LDH) | Nhồi máu cơ tim
Bệnh lý gan Ung thư |
| Lipase ( LPS) | Viêm tụy cấp |
| Trypsin ( TRY) | Viêm tụy cấp |
1.3.1. Enzym trong các bệnh tim mạch
– Creatin kinase (CK) là enzym dimer gồm 2 tiểu dơn vị (B kiểu não và M kiểu cơ), môi tiểu đơn vị có trọng lượng phân tử khoảng 40.000, là sản phẩm của các gen trên nhiễm sắc thể 14 và 19. Có 3 dạng isozym của CK: CK-BB dạng não (CK-1), CK-MB dạng lai (CK-2) và CK-MM dạng cơ (CK-3). Các isoenzym này khu trú khác nhau trong các mô . Cả 3 loại isoenzym được tìm thấy trong bào tương tế bào, bổ sung cho ba đồng phân CK tế bào chất này là 2 đồng enzym creatin kinase ti thể, bao gồm dạng có khắp mọi nơi (mtCK1) và dạng tâm cơ sarcomeric mtCK (mtCK 2)
CK-BB được biểu hiện trong tất cả các mô ở các mức thấp và ít có liên quan lâm sàng . Ở cơ xương biểu hiện của CK-MM (98%) và CK-MB (1%). Ngược lại, ở cơ tim biểu hiện của CK-MM ở mức 70% và CK-MB ở mức 25 – 30 %.
Hoạt độ CK huyết thanh tăng trong tất cả các bệnh loạn dưỡng cơ tiến triển (đặc biệt là bệnh Duchenne), tăng cao nhất ở độ tuổi vị thành niên và thơ ấu (7 đến 10 tuổi) và có thể tăng trong thời gian dài trước khi bệnh có biểu hiện lâm sàng. Hoạt độ CK cao trong viêm cơ virus, viêm đa cơ và bệnh cơ đơn thuần..
Hoạt độ CK tăng rất cao trong sốt cao ác tính. Các bệnh tổn thương cơ xương như ly giải cơ vân cấp tính do hội chứng vùi lấp, cấu trúc cơ bị phá hủy nặng nề, hoạt độ CK huyết thanh tăng 200 lần so với giới hạn bình thường. CK cũng tăng trong can thiệp phẫu thuật, tiêm truyền trong cơ. Ngoài ra, một số thuốc cũng gây tăng hoạt độ CK huyết thanh. Hoạt độ CK huyết thanh có mối liên quan nghịch với hoạt động tuyến giáp. Khoảng 60% trường họp suy giáp có mức tăng trung bình của hoạt độ CK cao hơn 5 lần giá trị bình thường, mức tăng hoạt độ CK cao nhất được tìm thấy gấp 15 lần giá ữị bình thường.
Những thay đổi của hoạt độ CK và isozym CK-MB huyết thanh gặp trong nhồi máu cơ tim. ( xem trong chương 5).Một số trạng thái tim khác cũng gây tăng hoạt độ CK và CK-MB huyết thanh, bao gồm: sự khử rung cơ tim, phẫu thuật đặt thông phổi tim và thông động mạch vành, ghép tim, viêm cơ tim và nhồi máu phổi. Hiện nay, để chẩn đoán nhồi máu cơ tim cấp, một số xét nghiệm không enzym đặc hiệu tim được sử dụng như troponin I hoặc T.
– Lactat dehydrogenase
Lactat dehydrogenase (EC 1.1.1.27) là enzym vận chuyển hydro, xúc tác phản ứng oxy hóa L-lactat thành pyruvat với chất trung gian NAD+ như chất nhận hydro. Enzym có trọng lượng phân tử 134.000 và gồm 4 peptid thuộc 2 loại M (hoặc A) và H (hoặc B), mỗi loại chịu sự kiểm soát gen khác nhau khu trú ưên nhiễm sắc thể 11 và 12. Các tiểu đơn vị tạo thành 5 isozym của LDH, bao gồm: LDH-1 (HHHH; H4), LDH-2 (HHHM; H3M) LDH-3 (HHMM; H2M2), LDH-4 (HMMM; H1M3), LDH-5 (MMMM; M4). Isoenzym thứ 6, LDH-X (còn
gọi là LDHc) gồm 4 tiểu đơn vị X (hay C), có trong tinh hoàn người sau tuổi dậy thì. LDH thứ 7, gọi là LDH-6 cũng được tìm thấy trong huyết thanh của những bệnh nhân bị bệnh trầm trọng.- LDH có trong bào tương của tất cả tế bào cùa cơ. Nồng độ của enzym trong các mô khoảng 500 lần cao hơn so với trong huyết thanh. Các mô khác nhau chứa đựng thành phần isozym khác nhau. Cơ tim và hồng cầu có LDH-1 và LDH-2. Gan và cơ xương có LDH-4 và LDH-5. LDH trung gian tìm thấy ở lách, phổi, tế bào lympho và tiểu cầu. Sự tăng hoạt độ LDH huyết thanh trong các bệnh lý gan, có thể gấp 10 lần bình thường trong gan bị nhiễm độc , tăng tới 2 lần trong xơ gan, vàng da tắc mật. Trong đó LDH- 5 huyết thanh tăng đáng kể , Các bệnh ác tính có hoạt độ LDH huyết thanh tăng, gồm 70% bệnh nhân có di căn gan, 20% đến 60% bệnh nhân có di căn ngoài gan. LDH-1 tăng đáng kể trong u tế bào mầm tinh hoàn và buồng trứng (61% trường hợp.
LDH và isozym LDH 1 được dùng trong chẩn đoán và theo dõi nhồi máu cơ tim ( xem chương 5).
– Aspartat amino transferase (AST) EC 2.6.1.1
AST tìm thấy đầu tiên ở tim, gan, cơ xương và thận, nồng độ cao nhất ở tim, gan , cơ xương ( bảng 2.3). AST có trong bào tương và cả trong ty thể. ÁST cùng với Alanin aminotransferase (ALT) EC 2.6.1.2, thuộc nhóm aminotransferase nhưng ALT chỉ có trong bào tương. Enzym aminotransferase có cấu trúc dimer với 2 chuỗi polypeptid, vào khoảng 400 acid amin.xúc tác phản ứng trao đổi amin
Bảng 1.4. Hoạt độ Transaminase trong một số mô ở người
(số lần gấp so với trong huyết thanh, tính theo đơn vị U/L)
|
ÁST |
ALT |
|
|
Tim |
7800 |
450 |
|
Gan |
7100 |
2850 |
|
Cơ xương |
5000 |
300 |
|
Thận |
4500 |
1200 |
|
Tụy |
1400 |
130 |
|
Hồng cầu |
15 |
7 |
|
Huyết thanh |
1 | 1 |
Hoạt độ AST trong huyết thanh bình thường là: 6 – 37 U/L, tăng trong chẩn đoán nhồi máu cơ tim ( NMCT) ( xem trong chương 5), và cũng có ý nghĩa trong các bệnh gan và cơ xương.
1.3.2. Enzym trong các bệnh gan
Những enzym có ý nghĩa nhất trong bệnh gan bao gồm ; Aminotransferase: AST, ALT, Alkalin phosphatase (ALP), Gamaglutamyl transferase (GGT)
- Aminotransferase (xem phần trên và chương 5)
- Alkalin phosphatase (ALP) 3.1.3.1
Ở người, ALP có nhiều dạng tùy thuộc vào nguồn gốc bên trong cơ thể .
ALP có trong hầu hết các cơ quan của cơ thể và đặc biệt gắn với màng và bề mặt các tế bào của niêm mạc ruột non và ống lượn gần của thận, trong xương (tạo cốt bào), gan và rau thai. ALP gắn liền với sự vận chuyển lipid ở ruột non và vận chuyển calci ở xương. Mức độ của enzym trong máu phụ thuộc vào tuổi tác, giới tính hoặc nhóm máu. Nồng độ phosphatase kiềm trong máu cũng tăng gấp 2-4 lần khi mang thai. Mức độ bất thường của phosphatase kiềm trong máu có thể chỉ ra các vấn đề liên quan đến gan, túi mật hoặc xương. Các khối u thận và nhiễm trùng cũng như suy dinh dưỡng cũng cho thấy mức độ bất thường của phosphatase kiềm trong máu.
Trong huyết thanh người trưởng thành khỏe mạnh ALP có nguồn gốc chính từ gan, một phần từ xương và một lượng nhỏ của ruột non . ALP huyết thanh tăng trong bệnh lý gan-mật với bất kỳ sự tắc mật do nguyên nhân gì và tăng trong bệnh lý xương liên quan đến sự tăng của tạo cốt bào. Hoạt độ ALP trong tắc đường mật ngoài gan tăng nhiều hơn so với tắc mật trong gan. Tăng hơn 3 lần trong sỏi hay ung thư đầu tụy, có thể tăng gấp 10 đến 12 lần giói hạn trên và thường trở về bình thường sau phẫu thuật tắc mật. Sự tăng cũng xảy ra tương tự trên bệnh nhân ung thư gan nguyên phát hoặc ung thư di căn thứ phát. Các bệnh gan tác động đên tế bào nhu mô gan như viêm gan nhiễm khuẩn, hoạt độ ALP tăng trung bình (dưới 3 lần) hoặc không tăng. Hoạt độ ALP có thể tăng trong phản ứng vói thuốc, tăng 2-3 lần so với giá trị bình thường có thể thấy ở phụ nữ mang thai tháng thứ 3, (có nguồn gốc từ rau thai). Tăng hoạt độ ALP huyết thanh có thể mang tính gia đình do nồng độ ALP của ruột non tăng cao.
-. Glutamat dehydrogenase (GLDH)
Glutamat dehydrogenase (GLDH) CE.14.13. là enzym có nhiều ở ty thể tế bào gan. , cơ tim, thận và với số lượng nhỏ hơn ở các mô khác như não, cơ xương và tế bào lympho. Hoạt độ GLDH /HT ở người bình thường nam 9 – 40U/L, nữ 9 – 35 U/L, tăng 4-5 lần trong viêm gan mạn, tăng 2 lần trong xơ gan. GLDH tăng rất cao trong nhiễm độc halothane và một số độc tố khác. Chìa khóa chẩn đoán phân biệt là xác định nơi khu trú trong cơ quan và trong tể bào của enzyme vì enzym đặc hiệu của ty thể. Tuy nhiên GLDH có nồng độ cao ở vùng trung tâm của tiểu thùy gan hơn ở vùng ngoại vi. Sự phân bố này trái ngược với ALT (enzyme chủ yếu ở bào tương tế bào gan). Bởi vậy, sự giải phóng GLDH cho biết trước tình trạng hoại tử vùng trung tâm tiểu thùy gan
-. Gamma-Glutamyl Transferase-GGT (EC 2.3.3.2);
GGT còn được gọi là gamma-glutamyl transpeptidase. GGT xúc tác sự vận chuyển nhóm γ- glutamyl từ peptid và họp chất chứa nó đến chất nhận. Chất nhận γ -glutamyl là cơ chất, nó cũng liên quan đến chuyển hóa của glutathion. GGT có ở ống lượn gần của thận, gan, tụy và ruột. Enzym có trong bào tương (microsom). GGT là chỉ điểm nhậy đối với các bệnh lý gan mật. Tắc mật trong gan hoặc sau gan có hoạt độ GGT huyết thanh tăng 5 đến 30 lần giới hạn trên. GGT tăng trên những bệnh nhân ung thư gan nguyên phát hoặc thứ phát (di căn), và xảy ra sớm hơn và rõ rệt hơn so với các enzym gan khác. Trong viêm gan nhiễm khuẩn tăng trung bình (2-5 lần bình thường) cũng tăng ở người viêm gan do rượu và chủ yếu ở người nghiện rượu, ngộ độc thuốc như phenolbarbital . Thuốc và rượu ảnh hưởng đến cấu trúc của microsom. GGT huyết thanh tăng trong viêm tụy mạn tính và ung thư tụy (liên quan đến sự tắc mật trong gan), tăng 5 đến 15 lần giới hạn trên.
-. 5′-nucleotidase (EC 3.1.3.5)
5′-nucleotidase là một enzym xúc tác sự phân cắt phosphoryl của 5’nucleotid., và phân bố rộng rãi trong mô động vật có xương sống. Ở động vật có vú, enzym chủ yếu nằm trong màng sinh chất và vai trò chính là chuyển đổi nucleotide ngoại bào (ví dụ 5′-AMP), thành nucleoside tương ứng (ví dụ adenosine) , enzyme đóng một vai trò quan trọng trong quá trình chuyển hóa nucleotide. Xác định hoạt độ 5’nucleotidase trong máu thường được sử dụng làm chức năng gan ở những cá nhân có dấu hiệu của các vấn đề về gan. Sự kết hợp hoạt độ của 5’nucleotisase huyết thanh và phosphatase kiềm (AP) cực kỳ hữu ích trong chẩn đoán ở các bệnh rối loạn gan mật tắc nghẽn. Mức bình thường của 5’nucleotidase là 2-17 U/L.
Hoạt độ 5’nucleotidase /ht tăng trong (ứ mật), thiếu máu cục bô ở gan, viêm gan , Ung thư gan hoặc khối u, xơ gan, bệnh tuyến tụy. cungxtawng trong bệnh phổi, Ung thư buồng trứng, Viêm khớp dạng thấp, hoặc sử dụng một số loại thuôc (acetaminophen, halothane, isoniazid, methyldopa, nitrofurantoin)
1- Lactat dehydrogenase- LDH (EC 1.1.1.27)
Hoạt độ LDH tăng đặc biệt cao (10 lần so với giá trị bình thường) trong gan bị nhiễm độc kèm vàng da. LDH-5 huyết thanh tăng đáng kể ở những bệnh nhân K gan nguyên phát và thứ phát. LDH huyết thanh còn được dùng cho chẩn đoán nhồi máu cơ tim, thiếu máu huyết tán, u quá sản tế bào mầm buồng trứng, u tế bào mầm tinh hoàn, trong các bệnh lý gan. LDH-1 tăng đáng kể trong u tế bào mầm tinh hoàn và buồng trứng (61% trường hợp). Hoạt độ LDH được dùng trong theo dõi bệnh Hodgkin và u lympho không Hodgkin.
Trong tổn thương trực tiếp tế bào gan, có sự tăng điển hình các enzym bào tương như AST, ALT và LDH. Mặc dù vàng da là dấu hiệu chìa khoá trong lâm sàng tìm thấy trong viêm gan cấp, tuy nhiên thường không gặp ở một số loại viêm gan virus. Sự tảng hoạt tính AST >200U/L, hoặc hoạt tính ALT> 300U/L là dấu hiệu đặc hiệu và nhạy cảm của trên 90% trường hợp viêm gan cấp. ALP thường tăng trung bình và thường nhỏ hơn 3 lần giá trị giới hạn trên. Có thế tham khảo quy trình chẩn đoán khi ALP tăng theo hình 6.8.
-. Ornithine Carbamoyltransferase còn gọi là Ornithine transcarbamoylase (OTC) (EC 2.1. 3.3) ít được dùng
OCT là enzyme xúc tác phản ứng hình thành citrulline từ l-ornithine và carbamoyl phosphate. Ở động vật có vú, nó hầu như chỉ nằm trong ty thể của tế bào gan và là một phần của chu trình urê. Hoạt tính OTC trong huyết tương trong khoảng 111–658 pkat / L (3-8 U/L)., trung bình 272 pkat / L), và hoạt tính tăng tuyến tính với các hoạt động của alanin aminotransferase (ALT) và aspartate aminotransferase (AST) trong huyết thanh ở bệnh nhân bị bệnh gan mật.
1.3.3. Enzym tụy
– Amylase
Amylase EC.3.2.1.1. là enzyme xúc tác sự thủy phân của tinh bột thành đường. Amylase có trong nước bọt, nơi bắt đầu quá trình tiêu hóa hóa học của người và một số động vật có vú khác.. Tuyến tụy và tuyến nước bọt tạo ra amylase (alpha amylase) để thủy phân tinh bột trong chế độ ăn uống thành disacarit và được chuyển hóa bởi các enzyme khác thành glucose để cung cấp năng lượng cho cơ thể. Thực vật và một số vi khuẩn cũng sản xuất amylase.
Có 3 loại amylase
Bảng 1.5. Phân loại amylase
| α-amylase | β-amylase | γ-amylase | |
| Nguồn | Động vật, thực vật, vi khuẩn | Thực vật, vi khuẩn | Động vật, vi khuẩn |
| Mô | Nước bọt, tuyến tụy | Hạt giống, trái cây | Ruột non |
| Tác dụng thủy phân | Thủy phân liên kết α-1,4 glycosid bất kỳ | Liên kết α-1,4 glycosid thứ hai | Liên kết α-1,4 glycosid cuối cùng |
| Sản phẩm | Maltose, dextrin, v.v. | Maltose | Glucose |
| PH tối ưu | 5,6 – 5,8 | 5.4–5.5 | 4.0–4.5 |
- Trị số bình thường amylase trong máu: 22-80U/L.
- Trị số bình thường trong nước tiểu: 42-321U/L.
Hoạt độ amylase tăng viêm tụy mạn,nghiện rượu, ngộ độc rượu. Trong viêm tụy cấp hoạt độ amylase tăng gấp 4 đến 6 lần .Hoạt độ Amylase cũng tăng trong viêm tuyến nước bọt cấp tính hoặc mãn tính, trong quai bị. Viêm túi mật cấp hoặc sỏi ống mật chủ, suy thận giai đoạn cuối cũng là nguyên nhân gây tăng Amylase.
-Lipase
Lipase (LPS) EC 3.1.1.3 là enzym thủy phân triglyceridtao thành 2 acid béo và monoglycerid. Lipase có trong tụy , dạ dày , ruột non.Nồng độ LPS trông tuyến tụy gấp 5000 lần các mô khác và gấp 20000 lần trong huyết thanh. Trị số bình thường lipase ở người < 38U/L
Bảng 1.6. Hoạt độ lipase ở người bình thường
LPS tăng trong viêm tụy cấp,, tăng khoảng 4-8 giờ sau khởi phát bệnh , đạt đỉnh ở 12 – 24 giờ.
1.3.4. Enzym xương
-Alkalin phosphatase ALP ( xem trong enzym gan) . ALP có trong xương ( tủy cốt bào) gan , thận.
Trong các bệnh lý về xương ALP /Huyết thanh tăng, tăng cao nhất trong bệnh Paget. Thiếu vitamin D hoạt độ ALP tăng gấp 2-3 lần bình thường , ALP tăng trong ung thư xương, cường giáp, tăng nhẹ trong loãng xương.
2. Vitamin
Vitamin là một phân tử hữu cơ thuộc loại vi chất dinh dưỡng thiết yếu mà sinh vật cần với số lượng nhỏ để duy trì hoạt động đúng đắn của quá trình trao đổi chất. Các chất dinh dưỡng thiết yếu này cơ thể không thể tổng hợp đủ số lượng và do đó phải được thu nhận thông qua chế độ ăn uống.
Người Ai Cập cổ đại đã biết rằng cho một người ăn gan có thể giúp chữa bệnh quáng gà. Trong Thời đại Khám phá các vùng đất mới, các chuyến du hành trên biển ở tình trạng không được tiếp cận với trái cây và rau tươi trong thời gian dài, khiến các thủy thủ đoàn tàu mắc bệnh do thiếu vitamin. Năm 1747, bác sĩ phẫu thuật người Scotland, James Lind đã phát hiện ra thực phẩm họ cam quýt giúp ngăn ngừa bệnh scorbut, một căn bệnh đặc biệt mà collagen không được hình thành đúng cách, gây ra vết thương kém lành, chảy máu nướu răng, đau dữ dội và gây tử vong. Suốt cuối thế kỷ 18 và đầu thế kỷ 19, các nhà khoa học đã phân lập và xác định một số loại vitamin. Năm 1884, Takaki Kanehiro, nhận thấy bệnh beriberi ở các thủy thủ đoàn cấp bậc thấp, (những người thường không ăn gì ngoài cơm). Năm 1897 Christiaan Eijkman đã phát hiện việc cho gà ăn gạo không đánh bóng thay vì loại đã đánh bóng sẽ giúp ngăn ngừa một loại viêm đa dây thần kinh tương đương với bệnh beriberi. Ba mươi năm sau, năm 1929 chính ông và Frederick Gowland Hopkins nhận giải Nobel Sinh lý /Y học về những đóng góp trong việc khám phá ra vitamin. Năm 1930, Paul Karrer đã làm sáng tỏ cấu trúc chính xác của beta-carotene, tiền chất chính của vitamin A, và các carotenoid khác. Các nghiên cứu về carotenoid, flavins , vitamin A và B2 của Paul Karrer và Walter Haworth đã đoạt giải Nobel Hóa học năm 1937.
Ngày nay vitamin và các thực phẩm bổ xung là ngành công nghiệp rất phát triển
2.1. Phân loại vitamin
Dựa vào tính chât hòa tan của vitamin mà người ta chia thành hai nhóm chính: vitamin tan trong nước và vitamin tan trong dầu. Ở người có 13 loại vitamin: 4 loại tan trong dầu (A, D, E và K) và 9 loại tan trong nước (8 vitamin B và vitamin C). Một vài nước thống kê gồm 14 loại vitamin ao gồm cả cholin
2.1.1. Các vitamin tan trong dầu
Các vitamin tan trong dầu là các vitamin A,D,E,K. Các vitamin này thường có tác dụng như chất điều hòa sinh học hoặc chất chống oxy hóa (antioxidant). Sự hấp thu của các vitamin này phụ thuộc vào sự bài tiết của hỗn hợp dich mật. Thiếu hụt các vitamin này thường gặp ở những bệnh nhân rối loạn hấp thu các chất béo. Các vitamin tan trong dầu vận chuyển trong máu nhờ sự gắn kết với lipoprotein và các chất mang như protein. Chúng được đào thải qua thận sau khi được chuyển hóa thành các sản phẩm hòa tan, vì vậy các vitamin này có thể bị tích lũy trong cơ thể gây tình trạng nhiễm độc.
Bảng 2.1. Các vitamin tan trong dầu
| Tên | Danh pháp hóa học | Cho phép trong khẩu phần ăn * | Bệnh lý thiếu hụt |
| Vitamin A | Retinol, retinal,
Retinoic acid |
900 µg | quáng gà, khô mắt , khô da |
| Vitamin D2, D3 | Ergocalciferol Cholecalciferol | 5.0 µg–15 µg | Còi xương (người trẻ), nhuyễn xương (người trưởng thành) |
| Vitamin E | Tocopherol Tocotrienol | 15.0 mg | hồng cầu dễ vỡ, thiếu máu dung huyết |
| Vitamin K1, K2 | Phyloquinon Menaquinon | 120 µg | thời gian đông máu tăng, bệnh chảy máu ở trẻ em |
* theo RDA Recommended dietary allowance
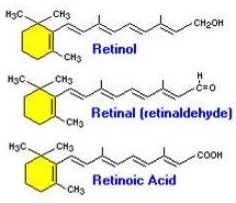
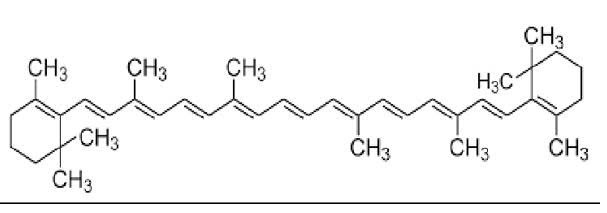
– Vitamin A – Vitamin A là chất dinh dưỡng thiết yếu của người. Nó là một nhóm các hợp chất hữu cơ bao gồm retinol (dạng alcol), retinal (dạng aldehyd) hoặc dạng acid retinoic và một số dạng tiền chất pro vitamin A. Các tiền chất của vitamin (tiền vitamin) tồn tại trong thực phẩm nguồn gốc thực vật gồm ba loại là α,β,γ – caroten có trong một vài loài cây trong họ Hoa tán.
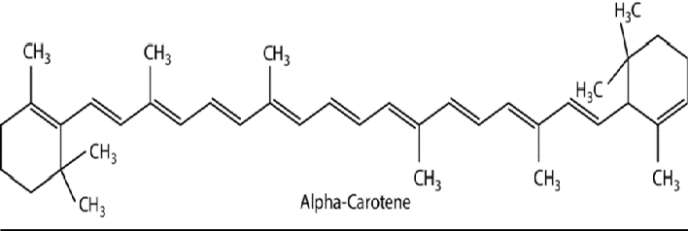
Vitamin A có nhiều chức năng quan trọng đối với sự tăng trưởng và phát triển, duy trì hệ thống miễn dịch và tốt cho thị lực. Vitamin A, dạng retinal kết hợp với protein opsin để tạo thành rhodopsin – phân tử hấp thụ ánh sáng , cần thiết cho cả với ánh sáng yếu (thị lực nhìn xa) và thị lực màu. Vitamin A dạng acid retinoic còn là chất cần thiết cho hoạt động của biểu mô, làm bài tiết chất nhày và ức chế sự sừng hóa.
Nhu cầu hàng ngày: người lớn: 5000 IU, có thai: 6-8000 IU. Tùy thuộc vào độ tuổi và giai đoạn phát triển của cơ thể mà số lượng Vitamin A cần thiết để nạp vào cơ thể khác nhau. Khuyến cáo nhu cầu Vitamin A thể hiện trong bảng 2.2 và 2.3.*
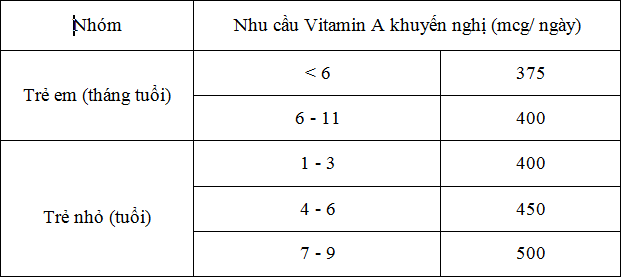
Bảng 2.2. Khuyến cáo nhu cầu Vitamin A dành cho trẻ nhỏ* ( mcg/ngày = μg/ngày)
*Bộ Y tế 2014
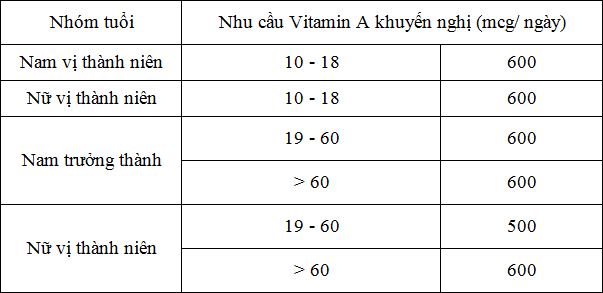
Bảng 2.3. Khuyến cáo nhu cầu Vitamin A dành cho tuổi vị thành niên và trưởng thành*
( mcg/ngày = μg/ngày)
*Bộ Y tế 2014
Nhu cầu Vitamin A dành cho các bà mẹ mang thai và cho con bú:
Phụ nữ trong quá trình mang thai cần bổ sung 800 μg/ngày Còn đối với phụ nữ đang cho con bú cần 850 μg/ngày .Vitamin A được tìm thấy trong nhiều loại thực phẩm nguồn gốc động vật dưới dạng retinol, trong thực vật dưới dạng carotene (tiền vitamin A). Gan, lòng đỏ trứng, bơ,dầu cá, sữa, pho mát, rau muống, rau ngót, rau cải xanh, bí đỏ, cà rốt, xoài có chứa nhiều vitamin A. Mỗi loại chứa ít nhất 0,15 mg (tương đương với 150 microgam hay 500 IU). Thiếu Vitamin A , biểu thị đầu tiên là thị lực suy giảm, giảm nhẹ thị lực gọi là quáng gà (khả năng nhìn giảm mạnh khi độ chiếu sáng thấp). Thiếu hụt liên tục sẽ sinh ra một loạt các thay đổi là bệnh khô mắt. Đầu tiên là khô màng kết do biểu mô của tuyến tiết nước mắt và nước nhầy bị thay thế bằng biểu mô keratin hóa. Tiếp theo là sự tích tụ các mảnh vụn keratin thành các mảng trong mờ nhỏ (đốm Bitot) và cuối cùng là sự ăn mòn bề mặt màng sừng thô ráp với sự thoái hóa và phá hủy của giác mạc (keratomalacia) và mù toàn phần. Thiếu vitamin A có thể gây suy giảm miễn dịch, giảm chiều dày lớp vảy ở da (các bướu nhỏ màu trắng ở nang tóc), bệnh da gà (Keratosis pilaris) và squamous metaplasia của biểu mô ở bề mặt của lối vào phía trên của hệ hô hấp và bàng quang, với lớp biểu mô bị keratin hóa
– Vitamin D.
Vitamin D là nhóm các secosteroid tan trong dầu, gồm 5 dạng từ vitamin D1 đến D5. Vitamin D1 (hợp chất của ergocalciferol với lumisterol): rất ít gặp, được tổng hợp thông qua phản ứng hóa học từ ergocalciferol (vitamin D2) và lumistrol trong cơ thể. Vitamin D2 (ergocalciferol), có trong thực vật (cỏ linh lăng và một số loại nấm :portobello, nấm hương, nấm mỡ). D2 hoạt thông qua phản ứng hóa học trong gan hoặc thận. Vitamin D3 (cholecalciferol), được tạo nên do bức xạ tia cực tím (UV) có bước sóng 270 đến 300 nm, sự tổng hợp xảy ra mạnh nhất ở bước sóng 295 đến 297 nm trên tiền chất 7-dehydrocholesterol. Người và động vật có xương sống, khi cơ thể tiếp xúc với ánh sáng mặt trời, khoảng 10000 đến 20000 IU vitamin D được tạo ra trong thời gian 30 phút trong da . Vitamin D4 (22-dihydroergocalciferol): hiếm gặp, được tạo nên nhờ phản ứng hóa học giữa các vitamin D2 với nhau, Vitamin D5 (sitocalciferol): cũng hiếm gặp , được tạo thành tương tự như D3 với thành phần 7- dehydrocholesterol .
Bảng 2.4. Các loại Vitamin D
|
Tên |
Thành phần hóa học |
Cấu trúc |
|
Vitamin D1 |
hợp chất
của ergocalciferol với lumisterol, 1:1 |
| Vitamin D2 | ergocalciferol (tạo thành từ ergosterol) | 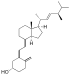 |
| Vitamin D3 | cholecalciferol (tạo thành từ 7- dehydrocholesterol ở dưới da). | 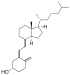 |
| Vitamin D4 | 22-dihydroergocalciferol | 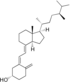 |
| Vitamin D5 | sitocalciferol (tạo thành từ 7- dehydrositosterol) | 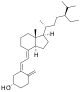 |
Vitamin D2 và D3 là 2 dạng có công dụng chính ở người. làm tăng cường khả năng hấp thu calci và phosphat ở đường ruột. D2 và D3 được đưa vào cơ thể qua việc ăn uống và các biện pháp bổ sung.
Chế độ ăn uống thiếu vitamin D và ít tiếp xúc ánh sáng mặt trời sẽ gây ra chứng nhuyễn xương (bệnh làm xương bị mềm, hay còi xương ở trẻ em). Thiếu vitamin D đã trở thành vấn đề toàn cầu đối với người già và vẫn còn phổ biến ở trẻ em và người trưởng thành. Nồng độ calcidiol (25-hydroxy-vitamin D) trong máu thấp có thể là hậu quả của việc tránh nắng.
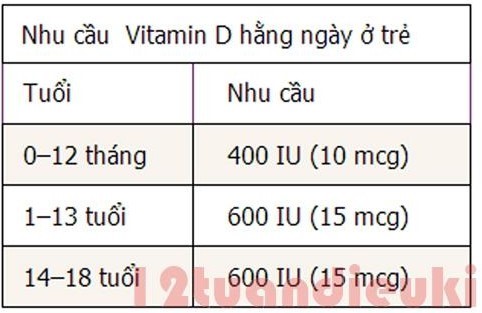
Bảng 2.5. Nhu cầu Vitamin D ở trẻ em
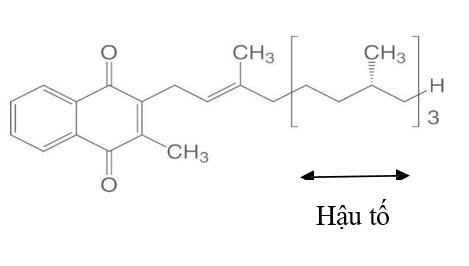
-Vitamin K
VitaminK là nhóm các vitamin tan trong dầu có vai trò quan trọng trong quá trình điều chỉnh , hỗ trợ đông máu, hỗ trợ sự trao đổi chất của xương và trao đổi chất của calci trong hệ thống mạch máu. Có hai loại vitamin K dạng tự nhiên: Vitamin K1 (phylloquinone) có trong thức ăn tự nhiên. có nhiều trong các loại rau xanh (cải, bông cải,…), dầu thực vật (dầu đậu nành), trái cây (bơ, kiwi, nho,…). Tuy nhiên, chỉ 5-10% lượng vitamin K1 từ nguồn thực phẩm được hấp thu ở đường tiêu hoá. Vitamin K1 giữ vai trò hoạt hoá yếu tố đông máu ở gan.
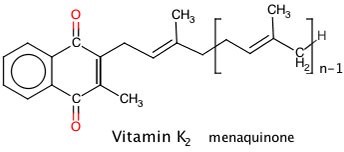
Vitamin K2 ( menaquinone) được tạo ra bởi các loại vi khuẩn có ích ở đại tràng, có nhiều dạng khác nhau: được biểu thị dưới dạng hậu tố (-n), thí dụ. MK-4 ( n=4 , 4 đoạn hậu tố), MK-7 ( n=7), Phổ biến nhất trong chế độ ăn uống của người là menatetrenone chuỗi ngắn, hòa tan trong nước (MK-4), được tạo ra bởi mô động
Vitamin K1 (phyloquinone)
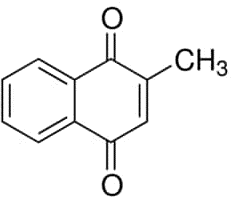
Vitamin K3 menadione
vật. Các chuỗi dài hơn MK-4 như MK-7, MK-8 và MK-9 chiếm ưu thế hơn trong thực phẩm lên men, chuỗi dài hơn (MK-10 đến MK-13) được sản xuất bởi vi khuẩn kỵ khí trong đại tràng , nhưng chúng kém được hấp thu và ít có tác dụng sinh lý.
Vitamin K3. được sản xuất tổng hợp , không có trong tự nhiên, không tốt cho sức khỏe, nó liên quan đến tổn thương gan và phá hủy các tế bào hồng cầu vận chuyển oxy. Hiện nay, vitamin này không được bán hợp pháp ở dạng bổ sung cho người, nó thường được sử dụng trong thức ăn cho gia cầm, gia súc, cũng như cho chó và mèo. Vitamin K3 tuy đã chứng minh có đặc tính chống ung thư và chống viêm trong các nghiên cứu trong ống nghiệm, mặc dù vậy, vẫn cần nghiên cứu thêm về tính an toàn hoặc hiệu quả của vitamin K3 trong điều trị ung thư hoặc các tình trạng khác ở người.
Vitamin K kích hoạt các protein trong quá trình đông máu, Tăng cường chức năng của tế bào nội mô mạch máu, chống xơ vữa động mạch, chống tắc nghẽn mạch, tránh nhồi máu cơ tim, đau thắt ngực. Kích hoạt protein osteocalcin, giúp gắn ion calci vào khung xương, ngăn ngừa loãng xương. Kanellakis S và cộng sự (2012) đã công bố hiệu quả của sự kết hợp calci, vitamin D3 và vitamin K2 (Trong một nghên cứu, bổ sung 800 mg calci, 10 mcg vitamin D3 và 100 mcg vitamin K2 ở 173 phụ nữ mãn kinh sau 12 tháng thử nghiệm, kết quả cho thấy mật độ khoáng trong xương cột sống của nhóm bổ sung tăng đáng kể so với nhóm đối chứng và cao hơn so với nhóm chỉ bổ sung calci và vitamin D3
-Vitamin E
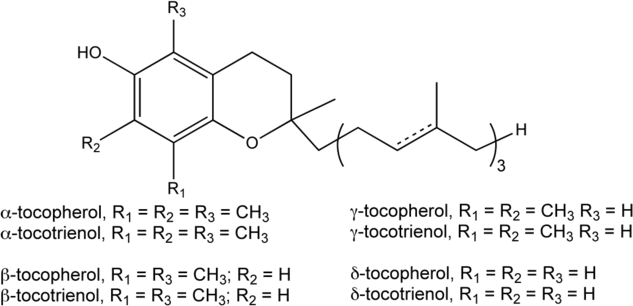
Vitamin E là tên gọi chung của các tocopherol và các tocotrienol. Chức năng chính của α-tocopherol trong cơ thể người là chống oxy hóa. Vitamin E tự nhiên tồn tại dưới 8 dạng khác nhau, trong đó có 4 tocopherol và 4 tocotrienol. Tất cả đều có vòng chromanol, với nhóm hydroxyl có thể cung cấp nguyên tử hydro để khử các gốc tự do Các tocopherol và tocotrienol đều có dạng alpha, beta, gamma và delta, được xác định theo số lượng và vị trí của các nhóm metyl trên vòng chromanol ( hình 2.5. Mỗi dạng có hoạt động sinh học khác nhau
Các loại Vitamin E
Vitamin E có trong các loại dầu thực vật như cọ dầu, hướng dương, ngô, đậu tương, ô liu. Các loại hạt hướng dương, các hạt ngũ cốc, cá, bơ, lạc, các loại rau lá xanh.. mầm lúa mì cũng là các nguồn cung cấp vitamin E..
Thiếu vitamin E có thể gặp ở trẻ đẻ non, người lớn bị cắt túi mật. Thiếu Vitamin E kéo dài sẽ có các triệu chứng thần kinh như: thất điều, yếu cơ, rung giật nhãn cầu, giảm nhạy cảm xúc giác. Vitamin E có tác dụng kháng vitamin K nên khi thiếu hụt có thể làm tăng nguy cơ của các vấn đề đông máu. Dùng Vitamin K liều cao (trên 3000 IU mỗi ngày) có thể gây rối loạn tiêu hóa (buồn nôn, đầy hơi, đi lỏng, viêm ruột hoại tử). Tiêm tĩnh mạch liều cao có thể gây tử vong.
(Khuyến cáo nhu cầu vitamin E (xem bảng phụ lụcậ
2.2. Các vitamin tan trong nước
Các vitamin tan trong nước bao gồm các loại vitamin B, vitamin C. Các vitamin tan trong nước dễ dàng hòa tan trong nước và nói chung là dễ dàng đào thải ra khỏi cơ thể, chúng không được lưu trữ vì vậy lượng tiêu thụ đều đặn là rất quan trọng. Đa số các vitamin tan trong nước liên quan mật thiết đến các chất tiền thân của coenzym. Các vitamin tan trong nước dễ dàng hấp thu tại ruột non, được vận chuyển dễ dàng trong máu và được đào thải qua thận ở dạng không chuyển hóa.
Bảng 2.5. Các vitamin tan trong nước
| Tên | Danh pháp hóa học | Cho phép trong khẩu phần ăn * | Bệnh lý thiếu hụt |
| Vitamin B1 | Thiamin | 1,2 mg | Beri – beri, hội chứng Wernicke-Kosakoff |
| Vitamin B2 | Riboflavin | 1,3mg | Viêm miệng, viêm da, chứng sợ ánh sáng, |
| Vitamin B3 | Niacin, niacinamid | 16mg | Pellagra |
| Vitamin B5 | Pantothenic acid | 5mg | Hội chứng Burning feet |
| Vitamin B6 | Pyridoxin
Pyridoxamin Pyridoxal |
1,3-1,7mg | viêm da, động kinh, thiếu máu nhược sắc |
| Vitamin B7 | Biotin | 30μg | Viêm da |
| Vitamin B9 | Folic acid Folinic acid | 400 μg | Thiếu máu nguyên hồng cầu không lồ, sai sot ống thần kinh |
| Vitamin B12 | Cyanocobalamin | 2,4 μg | Thiếu máu ác tinh, thiếu máu nguyên hồng cầu khổng lồ, bệnh lý thần kinh |
| Vitamin C | Ascorbic acid | 90 mg | Bệnh Scorbat |
* theo RDA Recommended dietary allowance
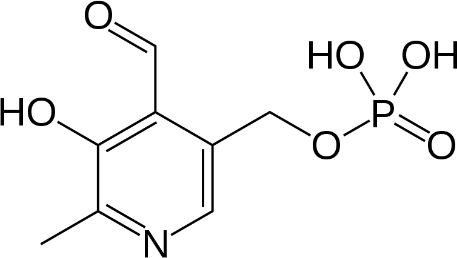
– Vitamin B1 ( thiamin)
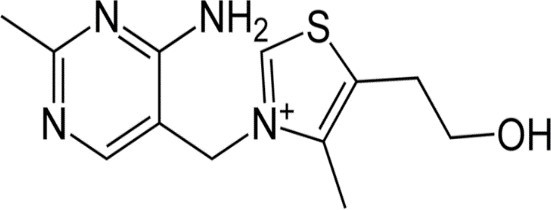
Thiamin (3 – [4 – amino – 2 – methyl – pyrimidyl – 5-methyl] 4 – methyl – 5 – [β-hydroxyethyl] thiazol), công thức hóa học C12 H17 N4 OS. Cấu tạo gồm một nhân pyrimidin mang nhóm amin, liên kết bằng cầu methylen với nhân thiazol .
Thiamin không màu, tan trong nước, methanol, và glycerol ; không tan trong aceton, ether, choroform, và benzen, không bền với nhiệt , tia cực tím và bức xạ gama; bền trong môi trường đông lạnh. Thiamin có thể bị phosphoryl hóa với 1,2 hoặc 3 gốc phosphat, dạng thường gặp là thiamin pyrophosphat (TPP) .
Thiamin
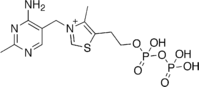
Thiamin pyrophosphat
Một lương nhỏ vitamin B1 và dẫn xuất phosphat của nó có trong đa số cây trồng và mô đông vật. Thiamin được tổng hợp ở vi khuẩn, một số đơn bào thực vật và nấm . Các nguồn thực phẩm có chứa thiamin như ngũ cốc, gan, tim, thận, thịt lợn nạc.
Thiamin được hấp thu ở ruột non bằng 2 quá trình: quá trình vận chuyển tích cực nhờ chất mang xảy ra ở nồng độ thấp ≤ 1μmol/L và bằng sự hấp thu thụ động ở nồng độ cao , tỷ lệ phần trăm hấp thu giảm theo sự tăng của nồng độ. Sau hấp thu được phosphoryl hóa thành thiamin pyrophosphat (TPP). Sự hấp thu thiamin tăng khi cơ thể thiếu hụt , giảm do hormon thyroid, đái tháo đường, uống rượu. Thiamin được vận chuyển qua tĩnh mạch cửa đến gan. Trong huyết tương thiamin được gắn với thiamin-binding protein chủ yếu là albumin.
TPP là dạng hợp chất chính trong tế bào, có khoảng 30mg vitamin được tích trữ trong cơ thể thì 80% ở dạng pyrophosphat , 10% ở dạng triphosphat và còn lại là monophosphat. Một nửa lượng dự trữ trong cơ xương còn lại là ở cơ tim, gan, thận và mô thần kinh ( não chứa nhiều dạng triphosphat).
Thời gian bán hủy của thiamin là 9,5 – 18,5 ngày và đào thải trong nước tiểu dưới dạng: 2-methyl-4-amino-5-formylaminopyrimidin, thiamin acetic acid, 2-methyl-4-amino-5-pyrimidin carboxylic acid và 4- methylthiazol-5-acetic acid.
TPP là coenzym của các enzym khử nhóm carboxyl trong phức hợp đa enzym Pyruvat dehydrogenase . Thiếu Vit B1, chuyển hóa của pyruvat và các ceto acid bị ngừng chệ gây bệnh lý như tê phù. TPP cũng là coenzym của transcetolase – enzym chuyển hóa carbohydrat theo chu trình pentose . TTP còn liên quan đến sự điều hòa các kênh ion, đặc biệt kênh clorid. TTP hoạt động như một chất cho phosphat trong sự phosphoryl hóa các protein.
Nhu cầu thiamin cần đáp ứng cho cơ thể phải đạt 0,40mg/1.000kcal; khi lượng này thấp hơn 0,25mg/1.000kcal thì sẽ gây nên bệnh tê phù Beriberi. Trên thực tế, nhu cầu vitamin B1 hay thiamin sẽ được đáp ứng thỏa mãn nhu cầu cho con người khi các loại lương thực cơ bản không xay xát trắng quá, chế độ ăn có nhiều hạt họ đậu. Trái lại, tình trạng thiếu vitamin B1 hay thiamin sẽ xảy ra khi sử dụng nhiều loại lương thực xay xát trắng, đường ngọt và rượu.
Khuyến nghị nhu cầu Vitamin B1 xem trong bảng phụ lục.
-Vitamin B2.( Riboflavin)
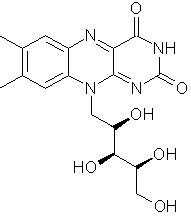
Vitamin B2, Riboflavin còn được gọi là vitamin H (7,8-dimethyl-10-[1’- D-ribityl] isoalloxazin), có công thức C17 H20 N4 O6 , phân tử gam :376,36g/mol, tan trong nước, được hấp thu dễ dàng, là thành phần của Flavin adenin dinucleotid (FAD), flavin mononucleotid (FMN) – coenzym của các enzym quan trọng trong chuyển hóa của acid béo, các chất cetonic, carbohydrat, và protein. Riboflavin có màu vàng hoặc màu da cam, được sử dụng như một chất màu thực phẩm.
Riboflavin
Riboflavin có nhiều trong gan, thận và tim. Sữa bò chứa phần lớn riboflavin tự do. Sữa nguyên chất có 14% flavin được gắn protein đặc trưng. Riboflavin bị phá hủy khi tiếp xúc với ánh sáng cực tím, sữa được đựng trong bình trong suốt sẽ có khả năng chứa ít riboflavin hơn sữa bán trong bình chứa đục. Trong lòng trắng và lòng đỏ trứng chứa riboflavin được gắn với các protein đặc biệt, để giúp việc phát triển của phôi .
Vitamin B2 được ăn dưới dang phức hợp protein với coenzym FMN và FAD . Các coenzym này được tách khỏi liên kết với protein bởi môi trường acid của dạ dày . Vitamin được tách ra dưới tác dụng của pyrophosphatase và phosphatase của ruột, được hấp thu nhanh ở ruột non, tương ứng với liều ăn hàng ngày là sấp xỉ 27 mg/ ngày. Muối mật làm dễ dàng hơn cho việc hấp thu. Ở nồng độ thấp được hấp thu bằng cách vận chuyển tích cực phụ thuộc ion natri và sự phosphoryl hóa. Trong máu flavin được vận chuyển bằng sự gắn lỏng lẻo với albumin và gắn chặt chẽ với các IgA, IgG và IgM. Khi có thai nồng độ các protein vận chuyển flavin tăng, dẫn đến kết quả là có tỷ lệ cao của flavin được hấp thụ trên bề mặt nhau thai.
Thiếu riboflavin thường cùng với thiếu hụt các vitamin khác, gây viêm miệng, môi nứt nẻ và nứt nẻ, đau họng, lưỡi đỏ và rụng tóc, ngứa mắt , chảy nước mắt, nhạy cảm ánh sáng. có liên quan đến thiếu máu đẳng sắc, hồng cầu bình thường
Bảng 2.6. Nhu cầu khuyến nghị vitamin B2 (Riboflavin)(mg/ngày)
– Vitamin B3 (Niacin)
Vitamin B3 (Niacin), còn có tên là vitamin PP , acid nicotinic. Công thức (C6H5NO2 pyridin -3-carboxylic acid,) là dẫn xuất của pyridin với nhóm carboxyl (-COOH).
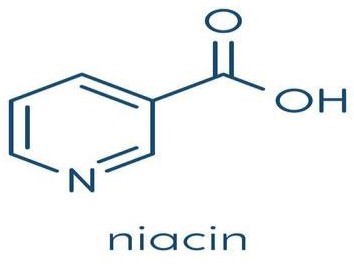
(Acid nicotinic) ( Nicotinamid)
Năm 1937 Juice Weidel nhận biết được vitamin B3 là “yếu tố ngăn ngừa Pellagra” một bệnh được khám phá lần đầu tiên năm 1755. Hai dạng hoạt động của niacin là nicotinamid adenin dinucleotid (NAD) và nicotinamid adenin dinucleotid phosphat (NADP), chúng có nhiều trong gan, tim , thận, gà, bò , cá ngừ, cá hồi, sữa , trứng, lê, trà là , cà chua, rau xanh, cà rốt, khoai tây tươi, măng tây, các loại hạt , đậu, nấm, men bia.
Các dạng NAD và NADP trong thức ăn đươc thủy phân ở đường tiêu hóa bởi NAD glycohydrolase có trong niêm mạc ruột non để tách nicotinamid . Ở nồng độ thấp , được hấp thu dễ dàng ở dạ dày và ruột non bởi cơ chế khuếch tán phụ thuộc Na+ và hấp thu theo cơ chế khuếch tán thụ đông khi ở nồng độ cao. NAD và NADP là coenzym vận chuyển điện tử trong chuỗi hô hấp tế bào.
Niacin ngăn cản sự phân hủy chất béo nên nó làm giảm mức acid béo tự do trong máu và do đó làm giảm tiết VLDL và cholesterol ở gan. do đó làm tăng mức lipoprotein tỉ trọng cao (HDL) hay cholesterol “tốt” trong máu. Đôi khi nó được chỉ định dùng cho người có HDL thấp và có nguy cơ cao bị đau tim.
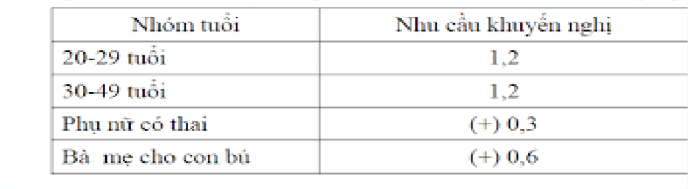
Khuyến nghị sử dụng hàng ngày đối với niacin là 2–12 mg/ngày đối với trẻ em, 14 mg/ngày với phụ nữ, 16 mg/ngày với nam giới và 18 mg/ngày đối với phụ nữ có thai và phụ nữ đang cho con bú.
Thiếu hụt niacin ở mức nhẹ làm chậm quá trình trao đổi chất, giảm khả năng chịu lạnh. Thiếu hụt nghiêm trọng trong chế độ ăn gây bệnh pellagra, với triệu chứng viêm da, tiêu chảy, sút giảm trí nhớ, tăng sắc tố, dày da, viêm miệng và lưỡi, rối loạn tiêu hóa có thể tử vong nếu không được điều trị. Các triệu chứng tâm thần thường gặp khi thiếu niacin bao gồm khó chịu, kém tập trung, lo âu, mệt mỏi, bồn chồn, thờ ơ và trầm cảm.
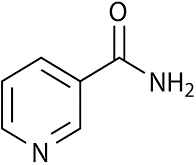
- Vitamin B5 (Acid Pantothenic)
Vitamin B5 được RJ Williams phát hiện vào năm 1933. Acid Pantothenic cần
Vitamin B5 (Pantothenic acid)
thiết cho sự hình thành coenzym-A có vai trò quan trọng trong trao đổi chất và tổng hợp cacbohydrat, protein, và mỡ. Về mặt lâm sàng, pantothenic acid cần thiết cho việc tổng hợp của các tế bào máu, sự trao đổi chất steroid, hoạt động của neuron và kích thích sản xuất kháng thể. Acid pantothenic có nhiều
trong pho mát, ngô, trứng, gan, thịt, lạc, đậu hà lan, đậu nành, men bia , mầm lúa mì. Vì sự phổ biến trong thức ăn nên việc thiếu pantothenic acid là rất hiếm,.
-. Vitamin B6
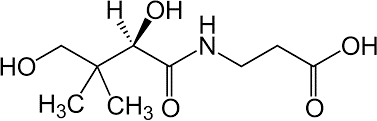
Vitamin B6 bao gồm 3 chất sau đây: Pyridoxin, pyridoxal, pyridoxamin
Năm 1934, Paul György (người Hungary) đã phát hiện ra một chất có thể chữa được bệnh viêm da acrodynia ở chuột, ông đặt tên là vitamin B6. Năm 1938, Richard Kuhn nhận giải Nobel Hóa học về carotenoid và vitamin, đặc biệt là B2 và B6. Cũng trong năm đó Samuel Lepkovsky đã phân lập được vitamin từ cám gạo. Một năm sau, Stanton A. Harris và Karl August Folkers xác định cấu trúc và tổng hợp được pyridoxine. Các nghiên cứu sâu hơn cho thấy pyridoxal, pyridoxamine và pyridoxine có hoạt tính gần như ngang nhau ở động vật, do hoạt tính vitamin của chúng phụ thuộc vào khả năng chuyển hóa chúng thành dạng pyridoxal-5-phosphate có hoạt tính enzym.
Pyridoxal phosphat (PLP)
PLP là coenzym của những enzym transaminase (ASAT, ALAT). PLP còn là coenzym của những enzym xúc tác phản ứng loại carboxyl, của những enzym tạo cystein. PLP cần thiết cho việc chuyển đổi tryptophan thành niacin, vì vậy tình trạng vitamin B6 thấp sẽ làm giảm sự tạo thành niacin.
PLP là coenzyme của glycogen phosphorylase, trong quá trình phân giải glycogen. PLP là một thành phần thiết yếu của enzym trong sinh tổng hợp các sphingolipid. PLP là một đồng yếu tố trong quá trình sinh tổng hợp năm chất dẫn truyền thần kinh quan trọng: serotonin, dopamine, epinephrine, norepinephrine và acid gamma-aminobutyric.
Thiếu vitamin B6 có thể xảy ra hiện tượng: ăn mất ngon, dễ bị kích thích mạnh, rụng lông tóc và một số triệu chứng đặc biệt ngoài da và niêm mạc. Ở trẻ em thiếu vitamin B6 thường chậm lớn và có thể có những cơn co giật. Người dùng liều cao và kéo dài INH cũng dẫn đến hội chứng thiếu vitamin B6.
Bảng 2.7. Nhu cầu vitamin B6 hàng ngày
| Tuổi | Vitamin B6 (mg/ngày)
Lượng khuyên dùng |
| 6-11 tháng | 0.4 |
| 12-23 tháng | 0.5 |
| 2-5 năm | 0.7 |
| 6-9 năm | 1.0 |
| 10-13 năm | 1.1/1.3 |
| Phụ nữ | 1.2 |
| Phụ nữ mang thai | 1.5 |
| Phụ nữ cho con bú | 1.6 |
| Nam giới | 1.6 |
Nạp quá nhiều vitamin B6 sẽ gây ngộ độc thần kinh.Vitamin B7
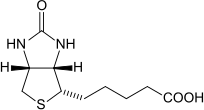
- (Biotin) hay vitamin H
Vitamin B7 rất quan trọng cho tóc và móng. giúp tóc mọc nhanh, khỏe và dày hơn.
Biotin
Trong thực phẩm biotin liên kết với protein. Dưới tác dụng của biotinidase, của dịch tuyến tụy giải phóng biotin và được hấp thụ ở ruột non, sự hấp thu nhạy cảm với tác dụng của các loại thuốc chống động kinh như carbamazepine và primidone. Hệ vi sinh vật ở đại tràng tổng hợp biotin ở dạng tự do ước tính tương đương với lượng biotin đưa vào chế độ ăn, rồi về gan. Người nghiện rượu giảm đáng kể biotin trong huyết tương
Biotin tham gia cấu tạo coenzym của các enzym: Acetyl-CoA carboxylase alpha (ACC1) Acetyl-CoA carboxylase beta (ACC2) chịu trách nhiệm chuyển bicarbonate thành acetyl-CoA, để thành malonyl-CoA cho tổng hợp acid béo ở bào tương. Biotin tham gia cấu tạo coenzym của Pyruvate carboxylase (PC) trong quá trình tạo gluconeogenesis (tổng hợp glucose), tham gia cấu tạo coenzym của Methylcrotonyl-CoA carboxylase (MCC) trong chuyển hóa leucine, tham gia trong Propionyl-CoA carboxylase (PCC) của chuyển hóa propionyl-CoA
Thiếu hụt biotin gặp ở những người thiếu dinh dưỡng protein năng lượng do ăn dài ngày lòng trắng trứng sống. Trong lòng trắng trứng sống, avidin -một glycoprotein liên kết mạnh với biotin, và chúng không được hấp thu.Thiếu hụt biotin biểu hiện viêm da bong, viêm lưỡi teo, tăng cảm, đau cơ, mệt nhọc, chán ăn, thiếu máu nhẹ , thay đổi điện tâm đồ và rụng tóc, móng giòn, dễ gãy.
Hàm lượng biotin cần thiết để hỗ trợ sức khỏe tốt theo độ tuổi như sau: Trẻ sơ sinh 0 – 6 tháng: 5 microgam / ngày; Trẻ 7 – 12 tháng: 6 μg / ngày; Trẻ 1 – 3 tuổi: 8 μg / ngày;Trẻ 4 – 8 tuổi: 12 μg / ngày; Trẻ dậy thì 9 – 13 tuổi: 20 μg / ngày ; Thanh thiếu niên 14 – 18 tuổi: 25 μg / ngày; Người lớn >19 tuổi: 30 μg / ngày; Phụ nữ mang thai: 30 μg / ngày; Phụ nữ cho con bú: 35 μg / ngày..
Chế độ ăn uống cung cấp mỗi ngày 150 – 300 microgam biotin được coi là đủ. Biotin có nhiều trong Thịt, lòng đỏ trứng, sữa, cá và loại quả hạt. Biotin bền vững khi đun nóng, nhưng kém bền trong môi trường kiềm.
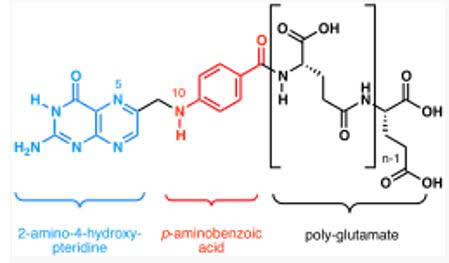
-Vitamin B9 ( acid Folic)
cần thiết trong quá trình sinh tổng hợp inosine monophosphate – tiền chất của GMP và AMP, tổng hợp methionine từ homocysteine, và chuyển hóa các acid amin cần thiết cho quá trình phân chia tế bào. Cơ thể người không thể tạo ra folate nên nó được yêu cầu trong chế độ ăn uống. Lượng folate được khuyến nghị hàng ngày dành cho người lớn ở Hoa Kỳ là 400 microgam từ thực phẩm hoặc thực phẩm chức năng. Acid folic cũng được phụ nữ sử dụng như một chất bổ sung trong thời kỳ mang thai để giảm nguy cơ khuyết tật ống thần kinh ở em bé. Mức độ thấp trong thời kỳ đầu mang thai được cho là nguyên nhân của hơn một nửa số trẻ sinh ra bị khuyết tật ống thần kinh . Hơn 80 quốc gia sử dụng bắt buộc hoặc tự nguyện tăng cường một số thực phẩm có acid folic như một biện pháp để giảm tỷ lệ khuyết tật ống thần kinh. Bổ sung lâu dài một lượng tương đối lớn acid folic có liên quan đến việc giảm phần nào nguy cơ đột quỵ .
Thiếu folate có thể do chế độ ăn uống không lành mạnh không đủ rau và các loại thực phẩm giàu folate khác; do một số rối loạn di truyền ảnh hưởng đến mức folate; và một số loại thuốc như phenytoin, sulfasalazine hoặc trimethoprim-sulfamethoxazole. Sự thiếu hụt folate tăng nhanh do uống rượu.
Thiếu folate có thể dẫn đến viêm lưỡi, tiêu chảy, trầm cảm, lú lẫn, thiếu máu, dị tật não và ống thần kinh của thai nhi. Thiếu folate được chẩn đoán bằng cách phân tích công thức máu đầy đủ , xác định nồng độ vitamin B12 và folate trong huyết tương. Nồng độ folate /HT < 3 μg / L là thiếu hụt. Nồng độ folate trong hồng cầu ≤ 140 μg / L là tình trạng không đủ folate.
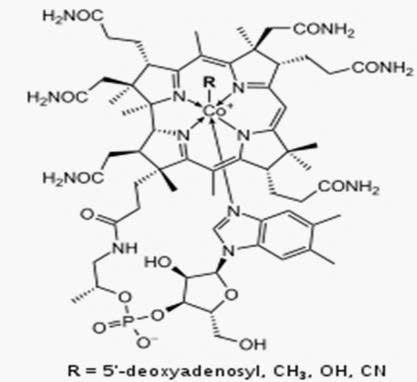
- Vitamin B12 (cobalamin),
Vitamin B12 là vitamin tan trong nước, có cấu tạo hóa học phức tạp nhất. Ở người là loại vitamin duy nhất phải có nguồn gốc từ thực phẩm hoặc chất bổ sung có nguồn gốc động vật vì chỉ một số vi khuẩn có thể tổng hợp vitamin B12.
Vitamin B12
(Cyanocobalamin) trong công thức với
Năm 1955, Todd biết được cấu trúc của vitamin B12 và nhờ đó ông đã nhận giải Nobel Hóa học năm 1957. Năm 1956 Dorothy Hodgkin xác định cấu trúc hoàn chỉnh của phân tử và bà đã được trao giải Nobel Hóa học năm 1964. Năm người đã được trao giải Nobel cho các nghiên cứu trực tiếp và gián tiếp về vitamin B12 gồm: George Whipple, George Minot và William Murphy (1934), Alexander R. Todd (1957), và Dorothy Hodgkin (1964).
Vitamin B12 có chức năng coenzyme. Ở người có 2 loại enzym cần B12 để hoạt động là Isomerase và Methyltransferase . Methylmalonyl coenzyme A mutase (MUT) là isomerase sử dụng dạng AdoB12, trong tổng hợp myelin , thiếu vitamin B12 gây suy giảm thần kinh. Methionine synthase, enzyme methyltransferase sử dụng MeB12 để chuyển nhóm methyl từ 5- methyltetrahydrofolate thành homocysteine, và tạo ra tetrahydrofolate (THF) và methionine.
Thực phẩm B12 được hấp thụ bằng quá trình khuếch tán thụ động (thường là một phần rất nhỏ trong tổng mức hấp thụ vitamin từ thức ăn) . Cơ chế hấp thụ tích cực rất phức tạp. Vitamin B12 gắn với protein và phải được giải phóng khỏi protein nhờ hoạt động của các protease tiêu hóa ở cả dạ dày và ruột non. Việc hấp thụ vitamin B12 trong thực phẩm đòi hỏi dạ dày, tuyến tụy ngoại tiết, yếu tố
nội tại và ruột non còn nguyên vẹn và hoạt động tốt. Các vấn đề với bất kỳ cơ quan nào trong số này có thể làm thiếu hụt vitamin B12.
Các thực phẩm chứa nhiều vitamin B12 là gan động vật, thịt, nội tạng trong đó có gan và thận của cừu rất giàu vitamin B12, ngao, loại động
vật có vỏ thuộc loài nhuyễn thể, cá mòi, cá hồi, thịt bò, ngũ cốc , các men dinh dưỡng tăng cường, trứng.
Nhu cầu vitamin B12 với người lớn được khuyến nghị là 2 μg/ngày. Phụ nữ có thai và cho con bú là 2,6 μg/ngày. Trẻ em chập chững biết đi khoảng 0,7 μg/ngày, thiếu niên khoảng 2 μg/ngày
Ở các nước phát triển nguyên nhân phổ biến nhất của thiếu vitamin B12 là do suy giảm khả năng hấp thu do mất yếu tố nội tại dạ dày , nguyên nhân thứ hai là do tuổi tác, suy giảm sản xuất acid chlorhydric, những người dùng thuốc kháng acid dài ngày, thuốc ức chế bơm proton, Chế độ ăn của người ăn chay và thuần chay có thể không cung cấp đủ B12 . Sự thiếu hụt vitamin B12 có thể được đặc trưng bởi bệnh thần kinh, các vấn đề về trí nhớ, giảm mức độ ý thức, sương mù não hoặc thiếu máu ác tính, một loại thiếu máu nguyên bào khổng lồ, Nếu không được điều trị ở trẻ sơ sinh, sự thiếu hụt có thể dẫn đến tổn thương thần kinh và thiếu máu. Nồng độ folate ở mỗi người có thể ảnh hưởng đến quá trình thay đổi bệnh lý và triệu chứng của sự thiếu hụt vitamin B12.
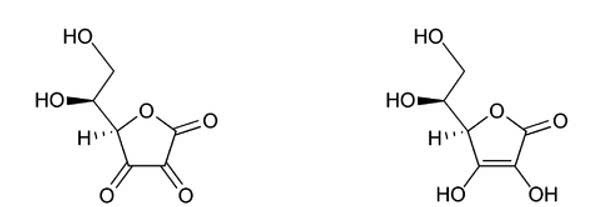
-Vitamin C – ascorbic acid
Vitamin C được phát hiện vào năm 1912, được phân lập vào năm 1928 và được tổng hợp vào năm 1933, trở thành vitamin đầu tiên được tổng hợp. Vitamin C ở dạng tinh thể trắng, rất dễ tan trong nước, tan trong ethanol 96, khó tan trong rượu, không tan trong ether và clorofom, và các dung môi hữu cơ, tồn tại được ở 100 °C trong môi trường trung tính và acid, bị oxy hóa bởi Oxi trong không khí và càng bị oxy hóa nhanh khi có sự hiện diện của Fe và Cu
Vitamin C dạng oxy hóa Vitamin C dạng khử
Vitamin C có nhiều trong các loại rau quả tươi ở phần cùi trắng của
cam, chanh, quýt, Hàm lượng trong rau quả phân phối không đều, có nhiều ở lớp vỏ hơn ở ruột, ở lá nhiều hơn ở cuống và thân rau, có hàm lượng cao trong rau xanh, đặc biệt là bông cải xanh, tiêu, khoai tây, cải brussel, rau cải, cà chua, cải xoong cam, quýt, chanh, bưởi. Cơ thể người không thể tự sản xuất vitamin C.
Thiếu vitamin C, có thể xuất huyết, vết thương lâu lành. Vitamin C tuy ít tích luỹ nhưng nếu dùng liều cao lâu ngày, có thể tạo sỏi oxalat (do dehydroascorbic chuyển thành acid oxalic), hoặc sỏi thận urat, có khi cả hai loại sỏi trên; rối loạn tiêu hóa; giảm độ bền hồng cầu. Dùng vitamin C liều cao kéo dài ở thai phụ gây tăng nhu cầu bất thường về vitamin C ở thai (vì vitamin C qua rau thai) dẫn đến bệnh scorbut sớm ở trẻ sơ sinh.
3. Các nguyên tố vi lượng
Nguyên tố vi lượng, là nguyên tố hóa học có nồng độ rất thấp (“lượng vết”). Chúng được phân thành hai nhóm: thiết yếu và không thiết yếu. Các nguyên tố vi lượng thiết yếu cần thiết cho nhiều quá trình sinh lý và sinh hóa ở cả thực vật và động vật. Các nguyên tố vi lượng thiết yếu ở động vật bao gồm Fe (hemoglobin), Cu (sắc tố hô hấp), Co (Vitamin B12), Mn và Zn (enzym). coban, đồng, flo, iốt, sắt, mangan và kẽm. Các nguyên tố vi lượng không chỉ có vai trò trong các quá trình sinh học mà còn là chất xúc tác để tham gia vào các cơ chế oxy hóa và khử… Mặc dù chúng rất cần thiết, nhưng chúng trở nên độc hại ở nồng độ cao. Các nguyên tố như Ag, As, Cd, Cr, Hg, Pb và Sn không có chức năng sinh học nào được biết đến, có tác dụng độc hại ngay cả ở nồng độ thấp .
3.1. Zn Kẽm
Kẽm là một kim loại lưỡng tính là nguyên tố vi lượng cần thiết cho cơ thể. mặc dù chỉ cần một lượng nhỏ. Kẽm không thể tự sản sinh ra trong cơ thể người, phải được bổ sung từ bên ngoài bằng thực phẩm chứa kẽm, thực phẩm chức năng, thuốc bổ sung kẽm. Trong huyết tương, kẽm vận chuyển ở dạng gằn với albumin (60%, ái lực thấp) và transferrin (10%). Kẽm là chất có phối hợp hình học linh động, các protein kết hợp với nó thay đổi cấu trúc protein nhanh chóng để thực hiện các phản ứng sinh học bằng cách tạo liên kết với 4 amino acid tạo thành các bộ phận của một số yếu tố phiên mã (transcription factor) – là các protein nhận dạng trình tự DNA trong quá trình phiên mã và sao chép DNA . Một nghiên cứu năm 2006 ước tính khoảng 10% protein người (tương đương khoảng 2.800 loại) có thể phụ thuộc vào kẽm và hàng trăm protein có chức năng vận chuyển kẽm
Kẽm được tìm thấy trong gần 100 loại enzym đặc biệt. Ở người , các enzym chứa kẽm là carbonic anhydrase và carboxypeptidase – các enzym cần thiết trong các quá trình của chuyển hóa cacbon dioxide (CO2) và tiêu hóa protein .
Nhu cầu hàng ngày:
Trẻ sơ sinh 1 – 6 tháng tuổi: 2 mg/ngày; 11 tháng tuổi: 3 mg/ngày; 1 – 3 tuổi: 3 mg/ngày;4 – 8 tuổi: 5 mg/ngày; 9 – 13 tuổi: 8 mg/ngày; >14 tuổi: nam 11 mg/ngày, Nữ 14 – 18 tuổi: 9 mg/ngày, > 19 tuổi : 8 mg/ngày Phụ nữ mang thai từ 18 tuổi trở lên: 11 – 12 mg/ngày- Phụ nữ đang cho con bú từ 18 tuổi trở lên: 12 – 13 mg/ngày
Kẽm có trong thức ăn động vật, sữa mẹ, ngũ cốc nguyên hạt. Thiếu kẽm gây liệt dương, vô sinh, suy nhược.
3.2. Đồng ( Cu)
Đồng là một nguyên tố vi lượng, có rất nhiều trong các loại thực phẩm. Cơ thể người chỉ cần một lượng đồng rất nhỏ để duy trì sức khỏe. Đồng là một thành phần quan trọng đối với sự phát triển của dây thần kinh, xương, các sắc tố melanin da, đồng thời có vai trò trong cấu trúc và hoạt động của nhiều loại enzyme như: enzyme cytochrome c oxidase, superoxide dismutase và dopamine beta hydroxylase
Đồng được hấp thụ trong ruột non và được vận chuyển tới gan bằng liên kết với albumin. Đồng vận chuyển chủ yếu trong máu bởi protein cerulolasmin. Bình thường cơ thể người lớn có từ 70 đến 100mg đồng. Sự hằng định phụ thuộc vào sự cân bằng giữa hấp thu ở ruột và thải trừ qua mật . Bệnh Wilson là bệnh di truyền, gây rối loạn chuyển hóa chất Đồng (Cu) trong cơ thể, đồng bị giữ lại chủ yếu ở gan và não. Bệnh được mô tả lần đầu tiên vào năm 1912 bởi BS Samuel Alexander Kinnier Wilson.
Bệnh nếu không được chẩn đoán và điều trị kịp thời dẫn đến sự tích lũy đồng trong cơ thể có thể gây ra các vấn đề nghiêm trọng, và có thể dẫn đến tử vong. Đây là một bệnh di truyền hiếm gặp với tỷ lệ mắc trung bình trên thế giới là 1/30.000 người. Tuy nhiên, tỷ lệ người mang gen bệnh là 1/100 người.
Người ta cho rằng kẽm và đồng là cạnh tranh về phương diện hấp thụ trong đường tiêu hóa vì thế việc ăn uống dư thừa một chất này sẽ làm thiếu hụt chất kia.. Người mắc bệnh tâm thần phân liệt ( bệnh schizophrenia) có nồng độ đồng cao hơn trong cơ thể. Tuy nhiên, hiện vẫn chưa rõ mối liên quan của đồng với bệnh này như thế nào (là nguyên nhân hay là hậu quả của bênh).
Theo tiêu chuẩn RDA của Mỹ về đồng đối với người lớn khỏe mạnh là 0,9 mg/ngày.
3.3. Selen (Se)
seleni lại là chất vi dinh dưỡng thiết yếu cho động vật
Ở người, seleni tồn tại dạng vết với chức năng cần thiết cho hoạt động của enzym chống oxy hóa như các glutathion peroxidase
Glutathion peroxidase (GSH-Px) xúc tác phản ứng phân hủy peroxid hydro:
GSH-Px
2 GSH+ H2O2 → GSSG + 2 H2O
Seleni cũng đóng vai trò trong hoạt động của các enzym deiodinase – enzym cần thiết cho việc chuyển thyroxin (T4) thành dạng hoạt động hơn
là triiodothyronin (T3). Thiếu hụt selen có thể có các biểu hiện giảm hoạt động tuyến giáp như mệt mỏi, trì độn tinh thần, bệnh bướu cổ, chứng ngu độn .
Selen có trong quả , ngũ cốc, thịt, cá và trứng
Thiếu hụt seleni là tương đối hiếm gặp. Tại Anh nhu cầu được khuyến cáo là
75 µg/ngày cho nam và 60 µg/ngày cho nữ. Thiếu hụt seleni có thể dẫn tới bệnh Keshan, làm cho cơ thể dễ bị mắc các bệnh do các nguồn gốc dinh dưỡng hay nhiễm trùng. là bệnh có tiềm năng gây tử vong.
Một số nghiên cứu còn tranh cãi
Một vài nghiên cứu cho rằng có liên quan giữa ung thư và thiếu hụt selen. Selen có thể giúp ngăn ngừa ung thư , có vai trò như chất chống oxy hóa hay bằng cách gia tăng hoạt động miễn dịch. Tuy nhiên chưa được thống nhất. Một thử nghiệm phòng ngừa bằng cách sử dụng liều lượng dinh dưỡng kết hợp các vitamin và khoáng chất chống oxy hóa để giảm các bệnh tim mạch và ung thư. SU.VI.MAX (Supplementation en Vitamines et Minéraux Antioxydants Study) kết luận rằng: bổ sung liều thấp (với 120 mg acid ascorbic, 30 mg vitamin E, 6 mg beta caroten, 100 µg seleni, 20 mg kẽm) làm giảm 31% tỷ lệ bị ung thư và giảm 37% mọi nguyên nhân gây tử vong ở nam, nhưng không có kết quả đáng kể đối với nữ. Seleni cũng được chứng minh là gia tăng hiệu lực điều trị, làm giảm độc tính của các thuốc hóa trị liệu và ngăn ngừa sức đề kháng của cơ thể với thuốc. Trong vòng 72 giờ thì hiệu lực của điều trị bằng các loại thuốc hóa học như Taxol và Adriamycin cùng với seleni cao hơn đáng kể so với chỉ dùng thuốc . Một nghiên cứu khác cũng chỉ ra rằng seleni có tác dụng ngăn chặn rủi ro phát triển bệnh đái đường (ĐTĐ) typ I. Tuy nhiên việc bổ trợ không được khuyến cáo cho những người ĐTĐ có dinh dưỡng đầy đủ.
3.4. Magiê ( Mg)
Cơ thể người trưởng thành có 22–26 gam magiê, 60% trong khung xương, 39% nội bào (20% trong cơ xương) và 1% ngoại bào. Magiê đựơc hấp thu và bài tiết qua đường tiêu hóa. Hàm lượng Mg nội bào tương quan với kali nội bào. Mg tăng làm giảm calci và có thể ngăn ngừa tăng calci huyết hoặc gây hạ calci máu. Mg trong chế độ ăn uống không được hấp thu được bài tiết qua phân; Mg hấp thụ được bài tiết qua nước tiểu và mồ hôi. Hơn 300 enzym cần Mg trong hoạt động xúc tác gồm các enzym tổng hợp ATP và tổng hợp DNA và RNA.
Mg có trong cám, hạt bí ngô, lúa mạch, bột kiều mạch, sữa chua , cá bơn, đậu garbanzo, đậu lima, đậu nành và rau bina. Đồ uống giàu magiê là cà phê, trà và ca cao. Nồng độ Mg huyết thanh ở người khoẻ mạnh theo khuyến cáo của hãng BeckmanCoulter: Nam: 0.73 – 1.06 mmol/L (1.8 – 2.6 mg/dL) Nữ: 0.77 – 1.03 mmol/L (1.9-2.5 mg/dL)
Magiê huyết tương thấp (hạ Mg huyết) là phổ biến: gặp khoảng 2,5–15% dân số nói chung. Từ năm 2005 đến năm 2006, 48 phần trăm dân số Hoa Kỳ tiêu thụ ít Mg hơn so với khuyến cáo trong chế độ ăn, do mất nước qua thận hoặc đường tiêu hóa, do điều trị bằng thuốc kháng acid ức chế bơm proton. Nghiện rượu liên quan đến tình trạng thiếu magiê. Nồng độ Mg huyết thanh thấp mãn tính có liên quan đến hội chứng chuyển hóa, đái tháo đường týp 2, rối loạn nhịp tim và tăng huyết áp
Khuyến nghị về chế độ ăn uống, Ở Anh, nhu cầu magiê được khuyến nghị hàng ngày là 300 mg đối với nam giới và 270 mg đối với phụ nữ. Tại Hoa Kỳ, khuyến nghị (RDA) là 400 mg đối với nam giới từ 19–30 tuổi và 420 mg đối với người lớn tuổi; đối với phụ nữ 310 mg đối với độ tuổi 19–30 và 320 mg đối với người lớn tuổi.. /.
Bài viết được tham khảo từ bài viết của PGS.TS.BS.Hoàng Thị Bích Ngọc



Bài viết liên quan
Chuyên đề 9: Sàng lọc trước sinh và sàng lọc sơ sinh
Chuyên đề 8. Hóa sinh các bệnh đường tiêu hóa
Chuyên đề 7 Hóa sinh lâm sàng bệnh gan
Chuyên đề 6. Sự hình thành bilirubin và các loại vàng da
Chuyên đề 5. Hóa sinh bệnh tim mạch
Chuyên đề 4. Chuyển hóa lipoprotein, các xét nghiệm lipid và lipoprotein